|
Odczynnik |
Próbka odniesienia (B) |
Roztwór wzorcowy (St) |
Próbka (S) |
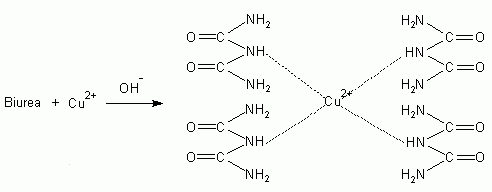
roboczy odczynnik do reakcji biuretowej |
400 µL |
400 µL |
400 µL |
wzorcowy roztwór białek |
- |
10 µL |
- |
próbka (osocze) |
- |
- |
10 µL |
woda dejonizowana |
10 µL |
- |
- |
Wymieszaj zawartość probówek i pozostaw na 30 min. w temperaturze pokojowej do zakończenia reakcji. Ustaw wartość transmitancji 100,0 dla próbki odniesienia, następnie zmierz transmitancję roztworów kalibracyjnych i próbki. Zastosuj diodę emitującą światło zielone (546 nm). Następnie oblicz wartości absorbancji.
Równanie do obliczenia stężenia próbki: Cs = As · |
Cst |
Ast |
Cs -
stężenie próbki
As -
absorbancja próbki
Cst -
stężenie roztworu wzorcowego
Ast -
absorbancja roztworu wzorcowego
DANE, ZMIERZONE WARTOŚCI, OBLICZENIA
Cst = _____________
Tst (zmierzona)= _____________ Ast (obliczona)= _____________
Ts (zmierzona)= _____________ As (obliczona)= _____________
Obliczenie stężenia białek: _____________
Wynik: Cs = _____________
Wartość podawana przez producenta: _____________
Błąd %
= _____________
Opracowanie: Sabina Povhe Lenart, Srednja šola za farmacijo, kozmetiko in zdravstvo, Ljubljana