|

SOČASNA DOLOČITEV KROMOVIH(III)
IN KOBALTOVIH(II) IONOV
Cilj
Namen tega poskusa je hkratno določanje kromovih(III) in kobaltovih(II) ionov v vzorcih vodnih raztopin z uporabo spektrometrične metode.
Uvod
1. Ozadje UV-VIS spektrometrije
Elektromagnetno sevanje, ki potuje skozi medij se lahko absorbira, odbije ali razprši. Do absorpcije pride, ko se energija sevanja ujema z energijsko razliko med dvema elektronskima energijskima ravnema v molekuli ali ionu, ki absorbira. To pomeni, da lahko elektron preide iz svojega osnovnega stanja v vzbujeno stanje. Pri elektronskem prehodu je energija sevanja navadno v razponu v območju med ultravijolično svetlobo (UV, 200 nm do 380 nm) in vidno svetlobo. Valovna dolžina absorbiranega sevanja je odvisna od elektronske razporeditve v molekuli ali ionu. V brezbarvnih (belih) snoveh so elektronske energijske ravni daleč narazen, zato absorbirajo sevanje z več energije (ultravijolično sevanje). V obarvanih spojinah so elektronske energijske ravni bližje druga drugi, zato takšne snovi absorbirajo vidno svetlobo.
UV-VIS spektrometrija uporablja ultravijolično in vidno svetlobo v analizne namene. Ta metoda se uporablja za študij spojin kot so:
- brezbarvne organske spojine, ki absorbirajo v UV območju (imajo elektrone tipa π ali ν, npr. aromatski ogljikovodiki, aldehidi, ketoni, karboksilne kisline, amini)
- nekatere brezbarvne anorganske spojine (npr. spojine redkih zemeljskih kovin, ozon, žveplov dioksid)
- obarvane organske spojine (ki imajo konjugiran sistem dvojnih vezi, npr. organska barvila)
- obarvane anorganske spojine (spojine prehodnih kovin kot so kalijev permanganat ali bakrov(II) sulfat)
- snovi, ki postanejo obarvane kot posledica kemijske reakcije (npr. tvorba kompleksnih ionov).
2. UV-VIS kot metoda za kvantitativno analizo
Intenziteta absorpcije elektromagnetnega sevanja je definirana z dvema parametroma: prepustnostjo ali transmitanco (T) in absorbanco (A). Prepustnost je definirana kot razmerje med močjo sevanja, ki je pripotovalo skozi vzorec (Φ) in začetno močjo sevanja(Φ0).
T = Φ/Φ0
Vrednost prepustnosti nam pove kakšen del sevanja, je pripotoval skozi vzorec. Prepustnost je navadno podana v odstotkih: T = Φ/Φ0·100 %. Absorbanca (A) je definirana z naslednjo enačbo:
A = log 1/T = - log T
Beer-Lamberov zakon pravi, da je za določeno valovno dolžino λ, absorbanca Aλ sorazmerna s koncentracijo c (v mol dm-3) snovi v raztopini, ki absorbira in dolžino poti sevanja skozi vzorec b (v cm)
Aλ = ελ·b·c
kjer je ελ sorazmernostni koeficient za valovno dolžino λ, znan kot molarni absorpcijski koeficient izražen v enoti dm3 mol-1 cm-1. Grafični prikaz absorbance nasproti koncentraciji je linearen, smerni koeficient premice pa ustreza ελ·b.
Če so v isti raztopini prisotni dve ali več snovi, ki absorbirajo, Beer-Lamberov zakon predvideva, da se za določeno valovno dolžino vrednosti posameznih absorbanc seštevajo:
A = A1+A2+A3+.....+An = (ε1·c1+ε2·c2+ε3·c3+.....+εn·cn)·b
Reagenti
- Kobaltov(II) nitrat heksahidrat, Co(NO3)2 · 6 H2O
- Kromov(III) nitrat nonahidrat, Cr(NO3)3 · 9 H2O
Material in oprema
- Spektrometer SpektraTM
- blistri
- plastenke opremljene s kapalnimi nastavki
- merilne bučke
25 cm3 in 50 cm3
Nevarnosti
|
Kobaltov(II) nitrat heksahidrat je strupen, lahko povzroča raka in alergije. Izogibajte se stiku s kožo in vdihavanju prahu. R: 42/43, 49, 50/53, 60, 68; S: 22, 36/37, 45, 53, 61. |
|
|
Kromov(III) nitrat nonahirdat drži oči in kožo, lahko okrepi požar. Preprečite stik z očmi in kožo. R: 8, 36/38; S: 26. |
 |
Postopek
1. Priprava standardnih raztopin
Ločeno pripravite standardne raztopine kobaltove in kromove soli v 50 cm3 merilnih bučkah s primernimi razredčitvami osnovnih raztopin v skladu s spodnji tabelo:
Co(NO3)2 · 6 H2O |
65 [g dm-3] |
|
Osnovni raztopini |
Cr(NO3)3· 9 H2O |
120 [g dm-3] |
Št. |
Co2+ |
Cr3+ |
V [cm3] |
c [mol dm-3] |
V [cm3] |
c [mol dm-3] |
1. |
0,5 |
|
5 |
|
2. |
1,5 |
|
10 |
|
3. |
2,5 |
|
15 |
|
4. |
3,5 |
|
20 |
|
5. |
4,5 |
|
25 |
|
Napišite vrednosti koncentracij v tabelo.
Namig: Izračunane vrednosti koncentracije v g dm-3 pretvorite v mol dm-3 tako, da jih delite z molsko maso ustrezne soli (kobaltova sol: M1=…………, kromova sol: M2=…………).
2. Izbira LED svetila
Odmerite 10 kapljic vsake raztopine št. 3 (kobaltove soli in kromove soli) v blistre. Izmerite prepustnost z modrim, zelenim in rdečim LED svetilom. Za vsako sol izberite LED svetilo, za katerega ste izmerili najnižjo prepustnost (absorbanca je torej najvišja). Kot slepo raztopino uporabite deionizirano vodo.
3. Merjene prepustnosti raztopin kobaltove in kromove soli pripravljenih v točki 1
Za vsako raztopino kobaltove soli (pet raztopin v tabeli pod točko 1, 10 kapljic vsake raztopine), opravite tri meritve prepustnosti z vsakim od LED svetil, ki ste jih izbrali pod točko 2 (za vsako raztopino morate skupno dobiti 6 meritev). Postopek ponovite tudi za raztopine kromove soli. Vpišite izmerjene vrednosti prepustnosti v tabelo in izračunajte vrednosti absorbance (po enačbi A = -log(T/100) ali poiščite vrednosti v tabeli, ki je priloga delovnega zvezka Izkustveni pristop k spektrometriji v vidnem področju). Kot slepo raztopino uporabite deionizirano vodo.
Meritve prepustnosti
Raztopina št. |
T (raztopina Co2+) |
T (raztopina Cr3+) |
LED 1 |
LED 2 |
LED 1 |
LED 2 |
1 |
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
4 |
|
|
|
|
|
|
|
|
|
|
|
|
5 |
|
|
|
|
|
|
|
|
|
|
|
|
Vrednosti absorbance (izračunane iz prepustnosti)
Raztopina št. |
T (raztopina Co2+) |
T (raztopina Cr3+) |
LED 1 |
LED 2 |
LED 1 |
LED 2 |
1 |
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
4 |
|
|
|
|
|
|
|
|
|
|
|
|
5 |
|
|
|
|
|
|
|
|
|
|
|
|
LED 1 – LED svetilo izbrano za raztopine kobaltove soli – barva .......................
LED 2 – LED svetilo izbrano za raztopine kromove soli – barva
.......................
4. Umeritvena premica
V spodnji tabeli vpišite koncentracije raztopin, nato pa še povprečne vrednosti absorbance izračunane na podlagi treh meritev (za LED 1 in LED 2). Podatke iz teh tabel uporabite za pripravo umeritvene premice , to je prikaz absorbance A kot funkcija koncentracije (A = f(c)). Za risanje grafa uporabite Microsoft Excel.
Tabela povprečnih vrednosti absorbance za raztopine kobaltove soli
Raztopina št. |
c [mol dm-3] |
A (povprečna) |
LED 1 |
LED 2 |
1 |
|
|
|
2 |
|
|
|
3 |
|
|
|
4 |
|
|
|
5 |
|
|
|
Tabela povprečnih vrednosti absorbance za raztopine kromove soli
Raztopina
št. |
c [mol dm-3] |
A (povprečna) |
LED 1 |
LED 2 |
1 |
|
|
|
2 |
|
|
|
3 |
|
|
|
4 |
|
|
|
5 |
|
|
|
5. Priprava in merjenje absorbance za dvokomponentno raztopino
Pripravite raztopine v skladu s spodnjo tabelo z uporabo 25 cm3 merilnih bučk (vsaka raztopina je mešanica kobaltove in kromove soli). Odmerite 10 kapljic vsake raztopine v blister in opravite 5 meritev za vsako raztopino z obema izbranima LED svetiloma. Izračunajte vrednosti absorbance kot v točki 4 in poiščite njihove povprečne vrednosti za vsako raztopino in obe LED svetili. Dobljene vrednosti vnesite v spodnje tabele. Kot slepo raztopino uporabite deionizirano vodo.
Osnovne raztopine |
Raztopina A |
Raztopina B |
V [cm3] |
V [cm3] |
Co(NO3)2· 6 H2O 65 [g dm-3] |
0,5 |
4,0 |
Cr(NO3)3 · 9 H2O 120 [g dm-3] |
2,5 |
10 |
H2O |
22 |
11 |
Rezultati meritev z LED 1
Meritev št. |
Raztopina A |
Raztopina B |
T |
A |
A
(povprečna) |
T |
A |
A
(povprečna) |
1 |
|
|
|
|
|
|
2 |
|
|
|
|
3 |
|
|
|
|
4 |
|
|
|
|
5 |
|
|
|
|
Rezultati meritev z LED 2
Meritev št. |
Raztopina A |
Raztopina B |
T |
A |
A
(povprečna) |
T |
A |
A
(povprečna) |
1 |
|
|
|
|
|
|
2 |
|
|
|
|
3 |
|
|
|
|
4 |
|
|
|
|
5 |
|
|
|
|
6. Izračun koncentracij Co2+ in Cr3+ ionov v raztopinah A in B
Odčitajte smerni koeficient (a) premice iz umeritvenega diagrama A = a·c
aCo2+, LED1=
aCo2+, LED2=
aCr3+, LED1=
aCr3+, LED2=
Za vsako raztopino izračunajte koncentracijo Co2+ in Cr3+ ionov, z uporabo spodnjega sistema enačb (vprašajte učitelja kako se ta sistem enačb izpelje).
ALED1 = aCo2+, LED1 · cCo2+ + aCr3+, LED1 · cCr3+
ALED2= aCo2+, LED2· cCo2+ + aCr3+, LED2 · cCr3+
7. Primerjava izmerjenih rezultatov s pričakovanimi rezultati
Izračunajte relativno napako (Δc) za koncentracije, ki ste jih določili raztopinam, ki vsebujejo Co2+ in Cr3+ ione (pod točko 6), z uporabo naslednje enačbe:
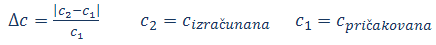
Poiščite pričakovane koncentracije na podlagi poznane sestave raztopin A in B (glej tabelo pod točko 5). Izračunane vrednosti koncentracij v g dm-3 preoblikujte v mol dm-3 tako, da jih delite z molsko maso ustrezne soli (kobaltova sol: M1=............, kromova sol: M2=............). Koncentracije izračunajte enako kot v točki 1.
8. Sočasno določanje neznane koncentracije Co2+ in Cr3+ ionov.
Analizirajte vzorec X z neznano koncentracijo Co2+ in Cr3+ ionov po postopkih, ki so opisani v točkah 5 in 6.
Meritev št. |
Vzorec X (LED 1) |
Vzorec X (LED 2) |
T |
A |
A (povprečna) |
T |
A |
A (povprečna) |
1 |
|
|
|
|
|
|
2 |
|
|
|
|
3 |
|
|
|
|
4 |
|
|
|
|
5 |
|
|
|
|
Pripravila: Tomasz Chmiel, Tomasz Dymerski, Technikum Przemysłu Spożywczego i Chemicznego w Gdańsku
Pregledal: Marek Kwiatkowski, Wydział Chemii Uniwersytetu Gdańskiego
|