|

1.
Učinek koncentracije reaktanta (CH3COO–)
na tvorbo kompleksa [Fe3(OH)2(CH3COO)6]+
Na blistru
pripravite raztopino slepe in preiskovane raztopine, ki vsebujejo različne
koncentracije železovih(III) in acetatnih ionov. Priprava raztopin je prikazana
v spodnji tabeli. Poskuse izvedemo s poenostavljenim pristopom odmerjanja
kapljic. Transmitance pripravljenih raztopin merimo proti slepi z uporabo modre
LED in izračunamo absorbance.
| |
Slepa |
Razt. 1 |
Razt. 2 |
Razt. 3 |
Razt. 4 |
|
FeCl3, 0,1 mol/L |
1  |
1  |
1  |
1  |
1  |
|
CH3COONa, 0,1 mol/L |
- |
1  |
2  |
3  |
4  |
|
Deionizirana voda |
8  |
7  |
6  |
5  |
4  |
|
n(Acetat)/n(Fe3+) |
- |
1 |
2 |
3 |
4 |
|
Absorbanca |
- |
0,025 |
0,052 |
0,166 |
0,264 |
1  (znak
za kapljico) približno 36 µl (znak
za kapljico) približno 36 µl
Rezultati
poskusa so predstavljeni na spodnjem grafu. Iz rezultatov lahko ugotovimo vpliv koncentracije reaktanta (CH3COO–) na tvorbo
kompleksa [Fe3(OH)2(CH3COO)6]+. Reakcija med železovimi(III) in acetatnimi ioni je značilna
ravnotežna reakcija. Pri stehiometričnem razmerju med reaktantoma n(Acetat)/n(Fe3+),
ko je to enako dve, se reaktanti le delno pretvorijo v produkte. Absorbanca
je razmeroma nizka. Znatno zvišanje absorbance pa opazimo pri nadaljnjih
poskusih. Večji izkoristek reakcije (višjo koncentracijo kompleksa) dobimo, če zvišujemo
koncetracijo acetatnih ionov. Ugotovimo, da se z dodajanjem acetatnih ionov
ravnotežje reakcije premika v smeri nastajanja produktov.
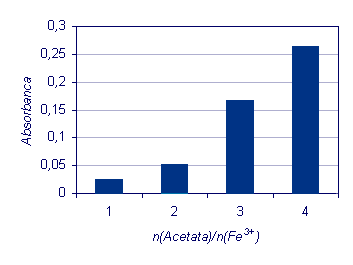
Razvila
in pripravila:
Nataša Gros, Univerza v Ljubljani, Fakulteta za kemijo in kemijsko tehnologijo
|