|

2.
Učinek dodajanja skupnih ionov (H3O+)
na tvorbo kompleksa [Fe3(OH)2(CH3COO)6]+
Slepo in
preiskovane raztopine pripravimo na blistru z dodajanjem ustreznega števila kapljic.
Vse preiskovane raztopine so
pripravljene tako, da je razmerje med železovimi(III)
in acetatnimi ioni 1:4. Raztopine se razlikujejo le v dodatku klorovodikove
kisline. Transmitanco merimo tako, kot je to opisano v prvem poskusu in izračunamo
absorbanco.
| |
Slepa |
Razt. 1 |
Razt. 2 |
Razt. 3 |
Razt. 4 |
Razt. 5 |
|
FeCl3, 0,1 mol/L |
1  |
1  |
1  |
1  |
1  |
1  |
|
CH3COONa, 0,1 mol/L |
- |
4  |
4  |
4  |
4  |
4  |
|
Deionizirana voda |
8  |
4  |
3  |
2  |
1  |
- |
|
HCl, 0,1 mol/L |
- |
- |
1  |
2  |
3  |
4  |
|
c(HCl) mmol/L |
- |
0 |
11 |
22 |
33 |
44 |
|
Absorbanca |
- |
0,264 |
0,202 |
0,126 |
0,063 |
0,023 |
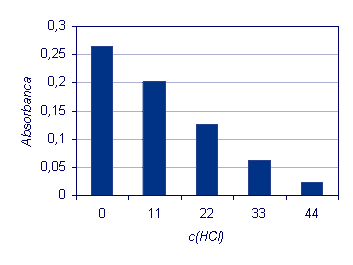
Rezultati, ki
so predstavljeni na spodnjem grafu, kažejo, kako dodatek oksonijevih ionov (H3O+)
vpliva na premik kemijskega ravnotežja reakcije. Dodajanje oksonijevih ionov
ima za posledico razgradnjo barvnega kompleksa in s tem premik ravnotežja reakcije
v smeri reaktantov. Višja je koncentracija oksonijevih ionov, izrazitejši je
premik ravnotežja reakcije v levo.
Razvila in pripravila: Nataša Gros, Univerza v
Ljubljani, Fakulteta za kemijo in kemijsko tehnologijo
|