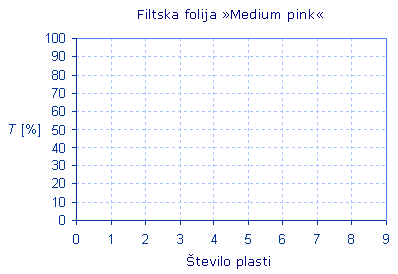
Rezultate vrišite v spodnji graf. Opredelite odvisnost transmitance od dolžine poti svetlobe (b) skozi absorpcijsko sredstvo. T ∝
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
KMnO4 je škodljiv ob zaužitju, vdihavanju ali pri absorpciji skozi kožo. Je močan oksidant in lahko zelo eksotermno reagira z organskimi snovmi. Uporabljajte laboratorijska očala in haljo ter se izogibajte stiku snovi ali njene raztopine s kožo. Snovi ne izpuščajte v okolje. |
|
Postopek
Poskus naredimo z devetimi raztopinami KMnO4 različne koncentracije. Raztopine pripravimo na blistru, kot je prikazano v preglednici. Transmitance merimo proti deionizirani vodi pri zeleni LED. Rezultate prikažemo grafično.

KMnO4( |
-* |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
H2O ( |
9 |
8 |
7 |
6 |
5 |
4 |
3 |
2 |
1 |
0 |
*Stolpec s modrim senčenjem označuje slepo.
Koncentracija osnovne raztopine KMnO4 je 10 mmol/L.
Rezultate vrišite v spodnji graf.
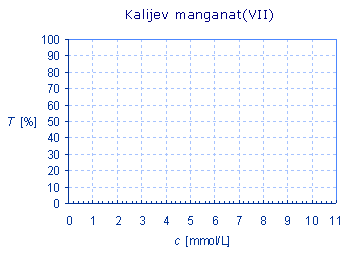
Zapišite zvezo med transmitanco (T) in koncentracijo snovi v raztopini (c).
T ∝
Poskus 3: Vpliv različnih snovi/specij na transmitanco
Cilj poskusa je pokazati, kako se spremeni transmitanca, če dikromat v raztopini pretvorimo v kromat.
Cr2O72– + 2 OH– |
|
2 CrO42–+ H2O |
(oranžen) |
|
(rumen) |
Nevarnosti
NaOH je koroziven, povzroča opekline oči in kože ter prebavil v primeru zaužitja. Izogibajte se stiku kemikalije s kožo in očmi, uporabljajte laboratorijska očala in haljo. |
|
K2Cr2O7 je zelo toksičen in nevaren za okolje. Stik s kožo lahko povzroči preobčutljivost, strupen je ob zaužitju. Uporabljajte zaščitne rokavice in očala, raztopin ne spuščajte v okolje. |
|
Postopek
Na blistru pripravite slepo ter pet raztopin dikromata. Pripravite tudi slepo ter pet raztopin kromata različnih koncentracij. Oba postopka priprave povzema preglednica. Uporabite osnovno raztopino K2Cr2O7 s koncentracijo 11 mmol/L, deionizirano vodo in raztopino NaOH s koncentracijo 2 mol/L.
|
Slepa |
Raztopine dikromata |
||||
K2Cr2O7( |
- |
1 |
2 |
3 |
4 |
5 |
NaOH ( |
- |
- |
- |
- |
- |
- |
H2O ( |
9 |
8 |
7 |
6 |
5 |
4 |
|
Slepa |
Raztopine kromata |
||||
K2Cr2O7( |
- |
1 |
2 |
3 |
4 |
5 |
6 NaOH ( |
2 |
2 |
2 |
2 |
2 |
2 |
H2O ( |
7 |
6 |
5 |
4 |
3 |
2 |
Transmitance raztopin dikromata oz. kromata izmerite s spektrometrom SPEKTRATM pri modri LED proti ustrezni slepi. Rezultate meritev sproti rišite v graf.
Rezultate vrišite v spodnji graf.
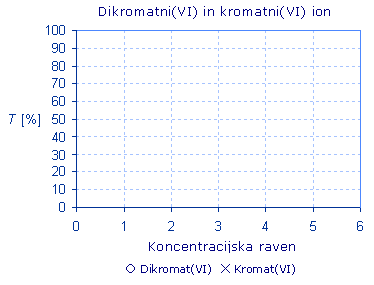
Če v eksponent zveze T ∝ e-cb uvedemo sorazmernostni faktor k, ki je značilnost snovi, dobimo končno formulo:
T =
V kemijski praksi niso zaželene eksponentne zveze med merjeno fizikalno količino in koncentracijo. Za praktično uporabo so najprimernejše linearne zveze.
Eksponentno zvezo T ∝ e-kcb lahko prevedemo v linearno tako, da jo logaritmiramo, naravni logaritem pa pretvorimo v dekadičnega. Nato namesto k/2,303 uvedemo molarni absorpcijski koeficient (ε) ter nov pojem - absorbanco (A). Dobljeno zvezo imenujemo Lambert-Beerov zakon.
A = ε c b |
Lambert-Beerov zakon
Simbol A označuje absorbanco, c množinsko koncentracijo specije (mol L-1), b pa je dolžina poti svetlobe skozi absorpcijsko sredstvo (cm). Simbol ε označuje molarni absorpcijski koeficient, ki velja za absorpcijo svetlobe neke specije pri določeni valovni dolžini in opredeljenih pogojih. Iz zgornje enačbe sledi, da je enota za molarni absorpcijski koeficient L mol-1 cm-1.
Dopolnite zvezo med absorbanco in transmitanco. (Absorbanca je s transmitanco povezana na enak način kot pH s koncentracijo oksonijevih ionov.)
A = ________T |
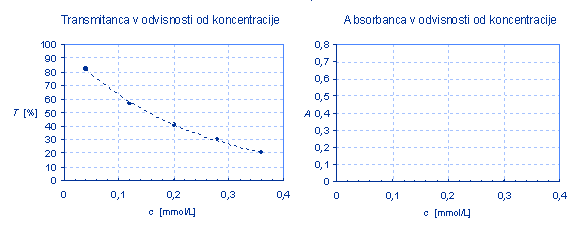
Iz transmitanc, ki so podane v tabeli, izračunajte absorbance. Transmitanco lahko izražamo kot delež od ena ali pa jo podajamo v odstotkih. Kadar s transmitanco računamo, mora biti izražena kot delež od ena.
c (mmol/L) |
0.04 |
0,12 |
0,20 |
0,28 |
0,36 |
T |
0,826 |
0,570 |
0,408 |
0,298 |
0,205 |
A |
|
|
|
|
|
Na sliki, ki sledi, so že vrisani podatki za transmitance. Vrišite vrednosti absorbanc pri posameznih koncentracijah.
Razvili in pripravili: Nataša Gros, Univerza v Ljubljani, Fakulteta za kemijo in kemijsko tehnologijo in Margareta Vrtačnik, Univerza v Ljubljani, Naravoslovnotehniška fakulteta