|

Uporaba kromatografskih tehnik za vrednotenje stopnje onesnaženosti tal s policikličnimi aromatskimi ogljikovodiki (PAH).
Cilj
Izolacija PAH frakcij iz tal, onesnaženih na različnih ravneh in določitev posameznih spojin.
Uvod
Policiklični aromatski ogljikovodiki so kemikalije, za katere je značilna razmeroma visoka toksičnost, pogosto kancerogenega značaja. Najbolj kancerogene spojine so benzopiren, benzoantrancen, dibenzoantracen, benzofluoranten, indeno (1,2,3-c,d) piren. PAH se presnavljajo v živih organizmih v metabolite, učinkovito vezane na DNA (npr. epoksidni derivati), ki vodijo do zelo verjetnih kancerogenih učinkov.
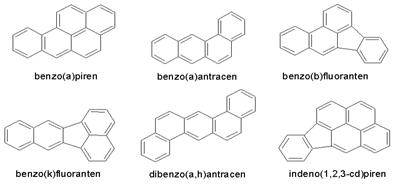
Slika: Izbrani policiklični aromatski ogljikovodiki
PAH so v okolju prisotni vedno kot večkomponentne mešanice, njihova sestava pa je odvisna od vira. Tvorijo se pri nepopolnem zgorevanju fosilov, med sežiganjem odpadkov in so tudi posledica različnih industrijskih dejavnosti, povezanih s pretvorbo olj in premoga. Najpogostejši vir tega onesnaženja v urbanem okolju je avtomobilskega izvora. Enako pogosti izvor, posebno med zimskim časom, so posamezni ogrevalni sistemi.
Okrog 90 % celotnih PAH v okolju, je zbranih v tleh. Koncentracije so v sledovih (ppm ali ppb)*, zato analizni postopki zahtevajo več stopenj. Vsaka od njih je enako pomembna za uspešno analizo, zato je treba vsako stopnjo (zlasti tiste, ki jih ni mogoče popraviti ali ponoviti) izvesti z veliko pazljivostjo in natančnostjo.
*ppm-parts per million, ppb-parts per billion.
Danes je tekočinska ekstrakcija najpogostejši način za izolacijo ogljikovodikov iz tal. Ekstrakcijo se nato izvede s topili nizke polarnosti, ki raztapljajo ogljikovodike: npr. n-heksan, cikloheksan, toluen, diklorometan, aceton in mešanica teh.
Večina pridobljenih komponent iz tal je nepolarnega ali nizko polarnega značaja. Polarne spojine pridobljene iz tal so običajno v manjšini. V neonesnaženih tleh so v glavnem verižni ogljikovodiki rastlinskega izvora, medtem, ko je v onesnaženem okolju mešanica nasičenih in aromatskih ogljikovodikov, v razmerju odvisnem od stopnje onesnaženosti.
Zelo pogost način za izolacijo PAH frakcij iz organskih ekstraktov, je uporaba tekočinske adsorpcijske kromatografije. V tem sistemu pride do ločitve zaradi različnih adsorpcijskih potencialov različnih komponent na adsorbent (v kromatografiji poimenovan stacionarna faza). Čim večja je afiniteta snovi do adsorbenta tem dlje se snov ob njem zadržuje in zato zapusti kromatografsko kolono kasneje. Več topila je treba (v kromatografiji imenovanega mobilna faza) za učinkovito spiranje takih spojin iz kolone (v kromatografiji poimenovano večji volumen zadrževanja). V nekaterih primerih je interakcija snovi in adsorbenta tako močna, da je treba uporabiti topilo z večjo elucijsko močjo (navadno bolj polarno).
Silikagel je eden najbolj uporabljanih anorganskih adsorbentov. Njegova površina je prekrita z aktivnimi silanolnimi skupinami (≡Si-OH) odgovornimi za adsorpcijo. Ker silanolne skupine precej lahko adsorbirajo polarne molekule (npr.vodo), vlaga lahko izrazito zmanjša njihovo aktivnost. Za dobro adsorpcijo aromatskih in alifatskih ogljikovodikov se uporablja brezvodni silikagel.
PAH določamo s plinsko kromatografijo (GC). V tej tehniki ločevanja snovi, zmes vstopa v plinsko mobilno fazo, medtem, ko stacionarna faza vsebuje tekočino z visokim vreliščem, kemijsko vezano na notranjost kolone. Substance v tem sistemu, se ločijo zaradi razlike v njihovi polarnosti od stacionarne faze, prav tako zaradi različnih temperatur vrelišča.
Najbolj uporabljen detektor v GC analizah ogljikovodikov, je plamenski ionizacijski detektor (FID).
Kemikalije
- Silikagel MN-Kieselgel 60- delci velikosti 0,08 mm.
- Petroleter.
- Toluen.
- Diklorometan.
- Brezvodni natrijev sulfat.
Aparature in pribor
- kovinska žlička,
- steklena bučka z zamaškom
- terilnica,
- tehtič 5-10 ml - 2 kosa
- 2 x erlenmajerica, 25 ml
- 3 x erlenmajerica 100 ml,
- steklen lij,
- filtrirni papir,
- 2 x destilacijska bučka 100 ml,
- 2 x destilacijska bučka 50 ml,
- 2 x destilacijska bučka 25 ml,
- cevasta steklena kolona s petelinčkom, notranji premer 1 cm, minimalna dolžina 15 cm,
- merilni valj 10 ml,
- 2 x merilni valj 25 ml,
- merilni valj 50 ml.
Nevarnosti
spojina |
R in S stavki |
oznake |
diklorometan
|
R: 40
S: (2-)23-24/25-36/37
|

|
petroleter
|
R: 45-65
S: 53-45
|
 
|
toluen
|
R: 11-38-48/20-63-65-67
S: (2-)36/37-62-46
|
 
|
Postopek
Iz 0 do 5 cm globine zemlje odvzamemo dva vzorca, 50 g vsakega. Vzorca odvzamemo s kovinsko žličko in ju damo v stekleni bučki s pokrovčkom. En vzorec vzamemo iz neonesnaženega območja (npr. iz parka ali gozda oddaljenega od virov onesnaženja), drugega pa iz onesnaženega območja (npr. z avtomobilskega parkirišča, z roba ceste). Ko vzorec prinesemo v laboratorij, damo tanko plast zemlje na filtrirni papir in odstranimo drobce rastlin in kamenčkov. Pustimo v suhem in temnem prostoru. Suho zemljo zdrobimo v terilnici, nato ocenimo maso suhe zemlje. Uporabljamo analitsko tehtnico, stariramo posodo in natehtamo 2-3 g podvzorce z natančnostjo, ne nižjo od 1 mg. Posodo z zemljo damo v peč in segrevamo na 105 °C, dokler ne dosežemo konstantne mase. Po naslednji enačbi izračunamo odstotek vode v zemlji.
% H2O = 100% x (mna zraku pos. zemlje[g] – mv peči pos. zemlje[g]) / mna zraku pos. zemlje[g]
Natehtamo približno 5 g (± 0,01 g) zemlje iz onesnaženega območja in približno 25 g (± 0,1 g) zemlje iz neonesnaženega območja. Natehtane vzorce damo v 100 ml erlenmajerico in dodamo 50 ml zmesi petroletra in diklorometana (3:2, V:V). Obe erlenmajerici damo v ultrazvočno kopel za 15 minut, ali pa na magnetnem mešalniku mešamo 20 minut. Odlijemo suspenzijo in filtriramo ekstrakt skozi filtrirni papir, zaščiten z brezvodnim natrijevim sulfatom . Filtriran ekstrakt zbiramo v destilacijski bučki in mu dodamo 0,2 ml toluena ter ga uparimo z rotavaporjem, kjer naj temperatura vodne kopeli ne presega 30 °C, do končnega volumna dodanega toluena (tanka plast ‘olja’ na notranji steni bučke). Nato dodamo 0,5 ml petroletra. V primeru težav s topnostjo ekstrakta bučko rahlo segrejemo v topli vodi.
V dve 25 ml erlenmajerici natehtamo dve porciji silikagela (2,5 g vsakega) in ju damo v peč na 150 °C za osem ur. Zapremo obe erlenmajerici in po hlajenju damo v vsako porcijo petroletra, tako, da sega plast topila do približno 1 cm nad gel. Rahlo pretresemo erlenmajerici, da odstranimo morebitne zračne mehurčke. Obe erlenmajerici hranimo zaprti vse do uporabe, da se izognemo izhlapevanju raztopine.
Na frito kolone damo krog filtrirnega papirja, erlenmajerico pa postavimo direktno pod izhod, da zbiramo topilo iz kolone. Rahlo zmešamo eno od porcij silikagela in jo počasi vlijemo v kolono skozi stekleni lij. Ko napolnimo kolono, damo krog filtrirnega papirja na vrh adsorbenta in dodamo 6 ml petroletra (ali več, dokler ne dosežemo konstantne višine gela - cca. 6 cm) ter zapremo izhod.
Zapomnimo si, da mora biti adsorbent vedno biti prekrit s plastjo topila!
Če je ekstrakt prej segret, ga ohladimo na sobno temperaturo. Odpremo petelinček in iztočimo petroleter do ne več kot 1-2 mm topila nad adsorbentom. Nato z brizgo ali pipeto v kolono previdno injiciramo ekstrakt na notranjo steno kolone ravno nad adsorbentno plastjo. Na izhod kolone damo kalibriran 25 ml valj.
Ko višina tekočine nad gelsko plastjo doseže 1-2 mm, previdno vlijemo na notranjo steno kolone 1 ml petroletra in počakamo, da spet doseže 1-2 mm nad sorbentom. Ta postopek ponovimo še enkrat. Nato zelo previdno vlijemo preostali petroleter (glede na podrobna navodila spodaj) in pričnemo z zbiranjem frakcije bogate z alifatskimi ogljikovodiki. Nato podstavimo pod izhod drugi valj in eluiramo s petroleter/toluensko zmesjo (9:1, V:V), da bi zbrali drugo frakcijo, ki vsebuje PAH.
Pogoji ločevanja:
- Aktiviran silikagel.
- Višina adsorbenta 6 cm.
- Volumen prve frakcije bogate z alifatskimi ogljikovodiki eluirane s petroletrom-12 ml.
- Volumen druge frakcije bogate s policikličnimi aromatskimi ogljikovodiki, eluirane s petroletrom in toluenom (9:1, V:V)-25 ml.
- Če je višina adsorbenta različna od 6 cm, se volumen zbranih frakcij sorazmerno spremeni.
- Damo PAH frakcijo v 50 ml destilacijsko bučko in jo koncentriramo na rotavaporju na volumen 1 ml. Pridobljen koncentrat shranimo v hladilniku, bučko ovijemo v aluminijasto folijo.
- Enako naredimo z drugim ekstraktom, vendar uporabimo svežo porcijo silikagela.
Analiza PAH:
Končna analiza PAH (po dodatku 2-metilantrancena kot internega standarda) s plinsko kromatografijo.
- Plinski kromatogram PAH izoliranih iz onesnažene zemlje.
- Plinski kromatogram PAH izoliranih iz neonesnažene zemlje.
- Plinski kromatogram standardne zmesi PAH nam da podatke za končni izračun.
Odčitamo čase, v katerih posamezni signali predstavljajo različne PAH, ki so prikazani na kromatogramu standardne zmesi (v kromatografiji so poimenovani retencijski časi). Tabela 1 predstavlja detekcijske koeficiente za PAH, ki so potrebni za nadaljnje kvantitativne izračune. Na osnovi retencijskih časov prepoznamo posamezne spojine na kromatogramu 1 in 2. Nato izmerimo višine kromatografskih signalov. Rezultate vpišemo v tabelo 1.
Po naslednji enačbi izračunamo vsebnost določenega PAH v frakciji:
manalite = mint.stnd. x fanalite x Wanalite / Wint.stnd.
m analite = m int.stand. x f analite x W analite/ W int.standard.
manalite– masa določenega PAH v frakciji
fanalite– detekcijski koeficient za določen PAH
Wanalite– višina kromatografskega signala določenega PAH [mm]
Wint.stnd.– višina kromatografskega signala internega standarda [mm]
Tabela 1: Rezultati določitev PAH v zemlji.
PAH |
f |
Vzorec 1 |
Vzorec 2 |
w [mm]
|
Masni delež [mg]
|
Masa v zemlji [mg/kg s.m.]
|
W [mm]
|
Masa v frakciji [mg]
|
Masa v zemlji [mg/kg s.m.]
|
2-Metilantracen |
---- |
|
|
--------- |
|
|
--------- |
Naftalen |
0,7 |
|
|
|
|
|
|
Fenantren |
0,7 |
|
|
|
|
|
|
Antracen |
1,2 |
|
|
|
|
|
|
Fluoranten |
0,8 |
|
|
|
|
|
|
Chrysene |
0,8 |
|
|
|
|
|
|
Benzoantracen |
0,9 |
|
|
|
|
|
|
Benzopiren |
1,2 |
|
|
|
|
|
|
Benzofluorantren |
1,0 |
|
|
|
|
|
|
Benzoperilen |
1,0 |
|
|
|
|
|
|
Celotni PAH |
|
|
|
|
|
|
|
Ob upoštevanju, da je bil ta delež dosežen z 80 % donosom in ob upoštevanju vsebnosti vode, izračunamo, koliko določenega PAH je prisotnega v zemlji. Rezultate podamo v mg/kg suhe mase.
Izračunamo celotne PAH, rezultate izrazimo v mg/kg suhe mase.
Primerjamo pridobljene rezultate s standardnimi vrednostmi kakovosti tal. Ocenimo raven onesnaženosti tal.
Standardi kakovosti, predstavljeni zemljo med drugim razvrščajo glede na vsebnost PAH (Direktiva Poljskega Okoljskega Ministrstva Dz. U. No. 165, 2002, 1359).
Skupine tal so opredeljene:
- Skupina A: Zemlje iz zaščitenih območij (zakonodaja o ohranjanju narave in vod).
- Skupina B: Kmetijska, gozdna in parkiriščna območja.
- Skupina C: Zemlje iz industrijskih in prometnih območij, izkoriščana območja.
Tabela 2 predstavlja standarde kakovosti za zemlje zaradi posebnih PAH vsebnosti (v mg/kg suhe mase).
Tabela 2: Referenčne vrednosti za devet PAH (mg/kg suhe mase) v prenasičeni zemlji iz treh skupin.
No |
PAHs |
Skupina A |
Skupina B |
Skupina C |
globina 0–0,3m |
globina 0–2,0m |
1 |
Naftalen |
0,1 |
0,1 |
50 |
2 |
Fenantren |
0,1 |
0,1 |
50 |
3 |
Antracen |
0,1 |
0,1 |
50 |
4 |
Fluoranten |
0,1 |
0,1 |
50 |
5 |
Chrysene |
0,1 |
0,1 |
50 |
6 |
Benzoantracen |
0,1 |
0,1 |
50 |
7 |
Benzopiren |
0,02 |
0,03 |
50 |
8 |
Benzofluorantren |
0,1 |
0,1 |
50 |
9 |
Benzoperilen |
0,1 |
0,1 |
50 |
10 |
Celotni PAH |
1,0 |
1,0 |
250 |
Kot celotni PAH je mišljen seštevek koncentracij naslednjih spojin: benzoantrancen, benzopiren, benzoflourantren in benzoperilen. V skladu s predloženim standardom kakovosti tal, se šteje za onesnaženo, ko vsaj ena spojina presega predpisano raven.
Pripravili: Fakulteta za kemijo, Univerza v Gdansku, Poljska
|