|

Določevanje vitamina E v sončničnem olju z uporabo HPLC
Namen
Namen eksperimenta je določiti vitamin E v sončničnem olju, z uporabo tekočinske kromatografije visoke ločljivosti HPLC.
Uvod
Beseda vitamini obsega veliko skupino nizkomolekularnih organskih spojin, z različno kemijsko strukturo, ki je široko zastopana v svetu rastlin in živali. Te spojine so pomemben faktor za rast in ohranjanje življenjskih funkcij. Za mnogo organizmov, vključno s človeškim, so običajno eksogenega značaja in morajo biti zagotovljeni skupaj s hrano. Negativne učinke na zdravje, ki jih povzroča pomanjkanje vitaminov imenujemo avitaminoza. Stanje med avitaminozo in normalnim stanjem vitaminov imenujemo hipovitaminoza. To stanje se lahko pojavi zaradi neprimerne diete, motene presnove vitaminov iz prebavnega trakta ali bakterijske infekcije. Prekomerna uporaba vitaminov, še posebno če so topni v maščobah povzroča škodljive učinke na organizem in jo imenujemo hipervitaminoza.
Vitamine delimo v dve skupini:
- topne v maščobah,
- topne v vodi.
Vitamin E
Vitamin E skupine imajo hidroksifenilno aromatsko enoto vezano na tetraizopentenilno verigo. Njihova raznolikost je posledica različnih pozicij CH3 skupin v strukturi.
Veliko vitaminov E vsebujejo pšenični kalčki, zelena solata, soja (veliko glicina).
Do sedaj je bilo izoliranih osem spojin, ki pripadajo dvema splošnima skupinama vitaminov E. Ti dve skupini sta tokoferoli in tokotrienoli.
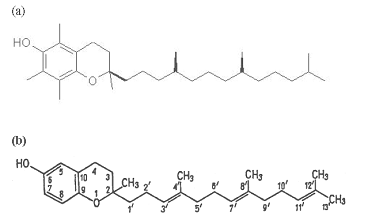
Kemijska struktura a) tokoferol, b) tokotrienol
Vitamini E so pri sobni temperaturi olja, netopna v vodi in lahko topna v maščobah. V odsotnosti kisika, so termično stabilni (nad 200 °C) in odporni na kisline in baze. Občutljivi so na UV svetlobo in kisik. V navzočnosti železovih soli, so podvrženi tvorbi dimerov, trimerov in kinonov. Njihova občutljivost narašča, z naraščajočim številom metilnih skupin v kemijski strukturi. Kadar uživamo zdravila, ki vsebujejo železo, vitamina E ne uporabljamo.
Vitamin E je odgovoren za nemoteno delovanje reprodukcijskega sistema pri mnogih vrstah živali. Do sedaj, ne poznamo negativnih učinkov pri ljudeh, pri katerih pride do pomanjkanja vitaminov E. Vitamin E ugodno vpliva na razvoj rdečih krvnih celic pri otrocih z anemijo. Priporočeni dnevni odmerek je 10-30 mg α-tokoferola. Vsebnost vitaminov E v prehranskih dopolnilih je ekvivalentno izražena z α-tokoferolom v mg. Čisti tokoferol ima 100 % bioaktivnost zato:
1 mg ekvivalentnega α-tokoferola = 1 mg čistega a-tokoferola
V praksi se uporablja tako naravni, kot sintetični tokoferol. Koncentrati vitaminov E se pridobijo iz rastlinskih olj (mešanica različnih tokoferolov z alfa tokoferolom). Zelo bogat vir teh vitaminov so rastlinska olja, posebno iz pšeničnih kalčkov, soje in bombažnih semen. Najdemo ga tudi v zeleni solati, špinači, zelju, maslu in jajcih.
Tekočinska kromatografija visoke ločljivosti (HPLC)
Tekočinska kromatografija je analitska metoda, ki se uporablja pri ločevanju zmesi. Analiti se med seboj ločijo zaradi različnih fizikalnih in kemijskih lastnosti. Analizirani vzorec raztopimo v primernem topilu (navadno v enakem kot je mobilna faza), glede na njegove fizikalno-kemijske lastnosti in izbran separacijski sistem. Nato raztopljen vzorec injiciramo v kolono. Spojine z višjo afiniteto do stacionarne faze, se premikajo počasneje, kot spojine z nižjo afiniteto. Na ta način pride do ločitve, kar omogoči prepoznavanje in določitev posamezne spojine tudi v zelo kompleksnih mešanicah. Mobilna faza predstavlja ustrezno izbrano topilo (eluent). Stacionarno fazo izberemo glede na polarnost. V novejših časih uporabljamo izraz normalna faza, to pomeni, da je stacionarna faza veliko bolj polarna od mobilne faze (silikagel-heksan). Pogosto se uporablja tudi izraz reverzna faza, ki pomeni, da je mobilna faza narejena iz silikagela, a je kemijsko modificirana in ima na površino vezane molekule ogljikovodikov, eluent vsebuje vodno mešanico topil s srednjo polarnostjo (oktadecil-silikagel-voda: acetonitril ali voda : metanol). Najbolj uporabljani detektorji pri HPLC so UV-VIS spektrofotometri. Vitamin E v svoji strukturi vsebuje kromoforje in absorbira sevanje pri določeni valovni dolžini, zato uporabljamo UV-VIS detektorje.
Višino ali ploščino kromatografskega vrha lahko povežemo z množino določane spojine.
Vitamine, ki so topni v maščobah, moramo najprej saponificirati.
Reagenti
- metanol (HPLC vrsta),
- acetonitril (HPLC vrsta),
- deionizirana voda,
- brezvodni natrijev sulfat,
- etanol (98 %),
- 0,5 M raztopina KOH v etanolu,
- petroleter,
- α-tokoferol.
Nevarnosti
Spojina |
R in S stavki |
Simboli |
Acetonitril |
R: 11; R:20/21/22-36
S: 1/2-16-36/37
|
 
|
Metanol |
R: 11-23/24/25-39/23/24/25
S: (1/2) 7-16-36/37-45
|
 
|
Etanol |
R: 11
S: 7, S: 16
|

|
0,5M raztopina KOH v etanolu |
R: 11
S: (1/2)-7-16-26-36/37/39-45
|

|
Fenolftalein
|
R:40
S: 36/37
|

|
Petroleter
|
R: 45-65
S: 53-45
|
 
|
α-
tokoferol |
Štejejo se kot nevarne kemikalije, ampak uporaba R in S stavkov, ter simbolov ni obvezna. |
|
Materiali
- lij ločnik (500 ml- 2 kosa),
- stekleni lij -4 kosi,
- destilacijska bučka,
- steklena bučka z zamaškom,
- steklena brizga (100 µl) 1 kos,
- bučka z okroglim dnom 100 ml 1 kos,
- vodna kopel,
- povratni hladilnik,
- merilni valj,
- filtrirni papir,
- membranski filter (0,45 mm),
- čaša 230 ml 2 kosa,
- aluminijasta folija.
Postopek
V bučko z okroglim dnom natehtamo 5 g (±0,01 g) sončničnega olja. Bučko ovijemo z aluminijasto folijo, da jo zaščitimo pred svetlobo. Dodamo 1-2 g askorbinske kisline in 60 ml 0,5 M raztopine KOH v etanolu. Namestimo povratni hladilnik in potopimo bučko v vodno kopel (95 °C). Reakcija saponifikacije mora potekati 45 minut. Po tem času raztopino prelijemo v lij ločnik. Bučko speremo z etanolom (3 krat po 5 ml) in ga zlijemo v lij ločnik. Dodamo mešanico deionizirane vode in etanola v razmerju 2:1, V:V.
Ekstrakcija vitamina E s petroletrom
Vitamin E ekstrahiramo s 70 ml petroletra. Ekstrakt prelijemo v drug lij ločnik in etanolno raztopino dvakrat ekstrahiramo s 50 ml petroletra. Zberemo vse ekstrakte, ne sme se tvoriti suspenzija. Ekstrakt speremo z vodo (4 krat 50 ml), dokler voda ne postane brezbarvna po dodatku 1 % fenolftaleina. Preostanek vode odstranimo z natrijevim sulfatom. Ekstrakt nato v rotavaporju uparimo do suhega (30°C). Preostanek raztopimo z 2 ml acetonitrila. Razdelimo na dva dela, prelijemo v steklenički (1 ml v vsako) in ju zapremo z zamaškom. Vsebino ene stekleničke direktno analiziramo s HPLC (3 krat ponovimo). V drugo dodamo 20 µl raztopine E vitamina in jo nato analiziramo s HPLC (3 krat ponovimo).
HPLC nastavitve
HPLC kolona C 18, pretok mobilne faze 0,8 ml/min, valovna dolžina l=292 nm, mobilna faza acetonitril/metanol 80:20 V:V.
Rezultati
Meritve območij signala, ki ga daje vitamin E v kromatogramu z dodatkom standarda in brez njega.Rezultate podamo v tabeli 1. Izračunamo koncentracijo vitamina E z uporabo enačb 1 in 2.
Tabela 1: HPLC rezultati
Ploščina vrha |
Meritev 1
|
Meritev 2 |
Meritev 3 |
Povprečna ploščina |
Brez dodatka standarda |
|
|
|
|
Z dodatkom standarda |
|
|
|
|
C = Y0· C s / ( Yi – Y0) |
(1) |
Y0= ploščina kromatografskega vrha vitamina E v vzorcu, brez dodatka standarda
Yi = ploščina kromatografskega vrha vitamina E v vzorcu, z dodatkom standarda
C = koncentracija vitamina E v vzorcu
C s = koncentracija vitamina E v standardu
Koncentracijo standarda izračunamo:
Vp= volumen vzorca
Cst =
koncentracija standarda
Vst = volumen standardne raztopine, ki je bila dodana vzorcu
Pripravili: Fakulteta za kemijo, Univerza v Gdansku, Poljska
|