|

Izolacija in identifikacija izbranih rastlinskih barvil
Namen
Vaja je namenjena izolaciji barvil ekstrahiranih iz rastlinskih materialov (posušena paprika, peteršilj) in njihovi nadaljnji separaciji in indetifikaciji, z uporabo tankoplastne kromatografije (TLC).
Uvod
Barvila (pigmenti) so opredeljeni kot različne kemične sestavine, ki absorbirajo elektromagnetno valovanje v vidnem območju (400-780 nm). Njihova prisotnost vodi k specifični barvi rastlin, živali in drugih objektov. Poznamo različne vrste barvil:
Naravna barvila so v sadju, zelenjavi ali vrtnih pridelkih (karoten, klorofil, antocianin), kot tudi v živalskih tkivih (npr. mioglobin, hemoglobin).
Umetna (sintetična) barvila niso prisotna v okolju, sintetiziral jih je človek (kinolinskorumeno).
Pri proizvodnji hrane se uporabljajo barvila, ki so enaka kot naravna. Imajo enako kemijsko strukturo, kot jo najdemo v naravi, le da jih je izdelal človek.
Naravna barvila delimo glede na kemijsko strukturo v dve skupini:
- karotenoidi - izoprenska barvila, klorofil, mioglobin, hemoglobin,
- anociani - flavanoidi in ostali.
Izoprenska barvila so derivati razvejanih ogljikovodikov, ki vsebujejo 40 ogljikovih atomov (imenujejo se tetraterpeni). Njihovo strukturo sestavljajo konjugirane dvojne vezi (polieni), skoraj vedno s trans konfiguracijo. To je glavni dejavnik, odgovoren za intenzivne barve teh snovi. Spojine se razlikujejo druga od druge zlasti po stopnji hidrogeniranosti, prisotnosti cikličnih struktur na obeh koncih ogljikovodikove verige, prisotnosti kisika v strukturi (ksantofili) ali njegovi odsotnosti (karoteni).
Lahko so aciklične (likopeni), monociklične (gama karoten) ali biciklične (alfa in beta karoten). Obarvanost karotenoidnih barvil se spreminja od rumene prek oranžne do rdeče. Prisotni so v rožah, sadju, semenih, koreninah.
Karotenoidi so eni izmed najbolj učinkovitih naravnih odstranjevalcev singletnega kisika, so antioksidanti in specifični biološki aktivatorji.
Kemijska struktura karotenoida.
Način, s katerim lahko izoliramo organske snovi iz rastlinskih materialov, je ekstrakcija trdno-tekoče. Ekstrakcija omogoča selektivni prehod iz trdne v tekočo fazo. Izkoristek ekstrakcije je odvisen predvsem od topnosti snovi, zlasti v topilu. Pogosto ekstrakcijo izvajamo v Soxhletovemu aparatu.
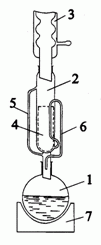
Soxhletov aparat: 1 bučka z okroglim dnom, 2 ekstraktor, 4 naprstnik, 3 kondenzator, 5 destilacijska cev, 6 povratna zanka, 7 ogrevalni plašč.
Pogosto mešanice barvil ločujemo s pomočjo kromatografskih metod. Poznamo kolonsko in plenarno tekočinsko kromatografijo. Pri tankoplastni kromatografiji (TLC), mobilno fazo razvijemo na ravni plošči. Stacionarna faza je narejena iz papirja ali tanke plasti sorbenta, ki je nanesen na stekleno ali aluminijasto ploščo.
Pri TLC se analiti, ki jih ločujemo, premikajo skupaj z mobilno fazo, ki se premika po stacionarni fazi. V tem primeru so analiti podvrženi dinamičnemu procesu absorpcije, desorpcije in delitve med obema fazama. Vsi ti procesi pripomorejo, da se analiti med seboj ločijo na posamezne komponente.
Določano sestavino, ki je prisotna v raztopini, nanesemo na TLC ploščo s stekleno kapilaro, v primerni oddaljenosti od roba plošče. Ploščo položimo v zaprto posodo, ki je nasičena s parami mobilne faze. Raztopina se premika po plošči navzgor zaradi kapilarnega vleka in tako povzroči migracije analitov vzdolž stacionarne faze. To imenujemo razvijanje kromatograma. Ko mobilna faza pride skoraj do vrha plošče, ploščo vzamemo iz posode, jo posušimo in ovrednotimo. Če posamezne komponente analita niso obarvane, jih pogosto lahko vidimo pod UV svetlobo.
Retencijski faktor Rf, ki opisuje razmerje časa porabljenega v stacionarni fazi in časa porabljenega v mobilni fazi, je pri TLC vrednost, ki opredeljuje določano spojino.
Rf= razdalja potovanja substance/razdalja potovanja tekočine.
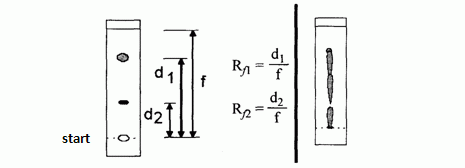
Primer TLC kromatograma dveh zmesi a) pravilno razvit kromatogram,
b) nepravilno razvit kromatogram.
Rf faktor ima vrednosti od 0 do 1. Če je Rf vrednost 0, se je snov premočno adsorbirala na stacionarno fazo. Če je Rf 1, pomeni, da stacionarna faza snovi ni zadrževala in je ta neovirano potovala z mobilno fazo. Optimalna vrednost Rf je med 0,2 in 0,8 in je odvisna od analita, vrste mobilne in stacionarne faze, zasičenosti posode s parami in temperature.
Reagenti
- posušena paprika,
- peteršilj,
- kloroform,
- aceton,
- petroleter,
- n-heksan,
- 10 % raztopina NaCl,
- CaCO3,
- brezvodni natrijev sulfat,
- silikagel plošče (silikagel 60 Merck),
- E160 C (capsantin in capsorubin),
- E160 A (vsebuje beta karoten).
Nevarnosti
Spojina |
R in S stavki |
Simboli |
Aceton |
R: 36-66-67
S: (2-)9-16-26
|
 
|
Kloroform
|
R: 22-38-40-48/20/22
S: (2-)36/37
|

|
Petroleter
|
R: 45-65
S: 53-45
|
 
|
n-heksan
|
R: 38-48/20-51/53-62-65-67
S: (2-)9-16-29-33-36/37-61-62
|
  
|
Natrijev karbonat |
S: 22 |
|
Materiali in metode
- analitska tehtnica,
- Soxhletov aparat,
- rotavapor,
- kalibriran valj 200 ml-1 kos, 50 ml-3 kosi,
- terilnica,
- erlenmajerica 50 ml- 2 kosa,
- filtrirni papir,
- lij ločnik,
- destilacijska bučka 50 ml-1 kos, 100 ml z zamaškom-1 kos,
- cevna steklena kolona z zamaškom, notranji premer 1 cm, minimalna dolžina 15 cm,
- bombažna vata.
Postopek
Ekstrakcija barvila paprike
Natehtamo 10 g sušene paprike v ekstrakcijski tulec in jo zapremo z bombažno vato. Cev položimo v Soxhletov aparat. V bučko z okroglim dnom, položimo nekaj vrelnih kamenčkov in vanjo nalijemo 120 ml kloroforma. Bučko vstavimo v grelni plašč in jo spojimo
s Soxhletovim aparatom. V cev spustimo vodo za hlajenje in pričnemo s segrevanjem. Raztopina mora vreti 1,5-2 uri. Nato izklopimo gretje in ekstrakt prenesemo v destilacijsko bučko. Bučko priklopimo na rotavapor. Rotavapor izklopimo, ko v bučki ostane 10 % začetnega volumna.
Ekstrakcija barvila peteršilja
V terilnici stremo 5 g listov peteršilja. Med trenjem dodajamo mešanico acetona in petrol etra (22:3, V:V). Postopno dodamo še 0,5 g CaCO3. Mešanico filtriramo skozi filtrirni papir, ter filtrat zberemo v liju ločniku. Dodamo 20 ml petroletra in 20 ml 10 % raztopine NaCl in zmes 2-3 min močno stresamo. Ko se fazi ločita, odstranimo tisto, ki je na dnu. Fazo, ki ostane v liju ločniku trikrat speremo z destilirano vodo. Ekstrakt nato prenesemo v erlenmajerico in dodamo brezvodni Na2SO4, da odstranimo preostalo vodo. Ekstrakt prenesemo v bučko, ki jo priklopimo na rotavapor. Rotavapor izklopimo, ko v bučki ostane 20-30 % začetnega volumna.
TLC analiza
V posodo nalijemo mešanico n-heksana in acetona (7:3, V:V), tesno zapremo in pustimo stati 15 min. Izrežemo koščke TLC plošče v velikosti 4,5x8,5 cm. S svinčnikom označimo start in točke od 1-3. Točka 1- standard, točka 2-ekstrakt paprike, točka 3- ekstrakt peteršilja. S stekleno kapilaro na točke nanesemo 1-2 kapljici analita. Ko nanesemo vse tri, jih posušimo s toplim zrakom sušilnika za lase. Premeri točk ne smejo biti večji od 5 mm. Ploščo nato položimo v posodo in jo zapremo. Plošča mora biti obrnjena s startnimi točkami navzdol. Ko mobilna faza pride dovolj visoko, posodo odpremo, vzamemo ploščo iz posode in s svinčnikom označimo, do kje je tekočina prišla. S svinčnikom označimo tudi točke na kromatogramu. Kromatogram posušimo s toplim zrakom. Izračunamo Rf faktor. Na osnovi Rf faktorja prepoznamo izolirane spojine.
Pripravili: Fakulteta za kemijo, Univerza v Gdansku, Poljska
|