
Monitorowanie przebiegu procesu fermentacji alkoholowej – oznaczanie zawartości alkoholu w produkcie
CEL
Wyznaczenie krzywej wzorcowej i oznaczenie zawartości alkoholu w produkcie fermentacji. Wyrażenie wyników w procentach objętościowych (%obj).
WPROWADZENIE
W wyniku fermentacji alkoholowej, cukry ulegają przekształceniu w etanol. W procesie fermentacji wykorzystuje się najczęściej szczepy Saccharomyces cerevisiae i Saccharomyces ellipsioideus.
S.cerevisiae i inne szczepy drożdży winnych posiadają zdolność metabolizowania glukozy, zarówno w warunkach tlenowych jak i beztlenowych. Teoretycznie, w warunkach beztlenowych z 1 mola glukozy można otrzymać 2 mole etanolu i 2 mole CO2. W praktyce, wydajność procesu jest nieco niższa, ze względu na jednoczesne powstawanie pewnej ilości gliceryny i innych związków.
APARATURA I ODCZYNNIKI
- spektrometr SpectraTM
- mikropipety
- łaźnia wodna
- wzorcowy roztwór K2Cr2O7 (0,25 mol dm-3)
- wzorcowy roztwór H2SO4 (2,25 mol dm-3)
- etanol (96 % obj.)
PRZYGOTOWANIE ROZTWORÓW WZORCOWYCH
- K2Cr2O7 (0,25 mol dm-3): Odważ 3,675 g K2Cr2O7 i rozpuść w wodzie dejonizowanej. Przenieś roztwór do kolby miarowej o pojemności 50 ml i dopełnij wodą dejonizowaną do kreski.
- H2SO4 (2,25 mol dm-3): Odmierz pipetą 6 cm 3 H2SO4 do kolby miarowej o pojemności 50 ml i dopełnij wodą dejonizowaną do kreski.
ZAGROŻENIA
 |
Kwas siarkowy(VI) jest silnie żrący, powoduje poważne oparzenia. Silnie trujący. Szkodliwy w przypadku wdychania, spożycia i kontaktu ze skórą. Spożycie może prowadzić do śmierci. Kontakt ze skórą prowadzi do rozległych i poważnych oparzeń.
R:35
S: 26-30-36/37/39-35
|
 |
Dichromian potasu jest silnie trujący, niebezpieczny dla środowiska, szkodliwy w kontakcie ze skórą.
R: 49-46-21-25-26-37/38-41-43-50/53
S: 53-45-60-61
|
 |
Etanol jest łatwopalny.
R: 11
S: (2-)7-16
|
SPOSÓB POSTĘPOWANIA
Fermentator
- przygotuj fermentator do przeprowadzenia procesu biotechnologicznego w warunkach beztlenowych,
- przygotuj zawiesinę komórek drożdży: 10 g drożdży na 1 dm3 wodnego roztworu glukozy (10 %),
- zaopatrz fermentator w wylot do odprowadzania CO2,
- fermentacja powinna przebiegać w temperaturze 30°C.
Przygotowanie próbki do pomiarów
Po upływie czterech tygodni pobierz 10 cm3 próbkę zawartości fermentatora i przesącz ją w celu usunięcia komórek drożdży.
Napełnij zagłębienia blistra zgodnie ze wskazówkami w Tabeli 1.
Tabela 1:
|
VK2Cr2O7 [µL] |
VH2SO4 [µL] |
VH2O
[µL] |
Vetanol
[µL]
|
Próbka
[µL] |
Etanol
[%obj.]
|
Rozt. kal. 1 |
180 |
110 |
100 |
0 |
0 |
0 |
Rozt. kal. 2 |
180 |
110 |
96 |
4 |
0 |
3,84 |
Rozt. kal. 3 |
180 |
110 |
92 |
8 |
0 |
7,68 |
Rozt. kal. 4 |
180 |
110 |
88 |
12 |
0 |
11,52 |
Rozt. kal. 5 |
180 |
110 |
84 |
16 |
0 |
15,36 |
Próbka |
180 |
110 |
0 |
0 |
100 |
? |
Zmierz transmitancję roztworów za pomocą spektrometru SpectraTM używając diody emitującej zielone światło. Wartość transmitancji 100,0 ustaw dla próbki wody dejonizowanej (próbka odniesienia). Po zmierzeniu transmitancji oblicz wartości absorbancji i sporządź krzywą kalibracyjną absorbancja w funkcji %obj etanolu. Zmierz transmitancję próbki, oblicz wartość absorbancji i odczytaj zawartość etanolu z wykresu.
WYNIKI
Tabela 2: Transmitancja i absorbancja roztworów kalibracyjnych
Etanol
[% obj.]
|
0 |
3,84 |
7,68 |
11,52 |
15,36 |
T
[%] |
95,5 |
94,2 |
93,7 |
92,7 |
91,9 |
A |
0,01996 |
0,02604 |
0,02826 |
0,0329 |
0,0376 |
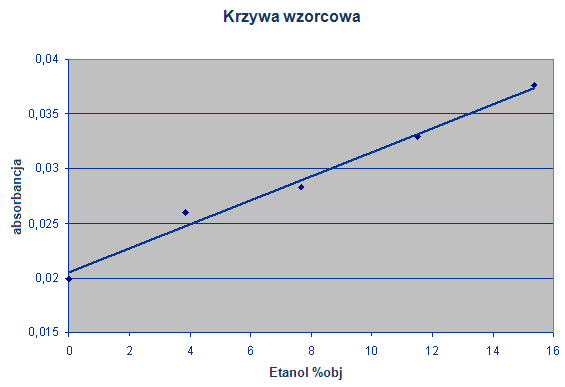
Wykres 1: Krzywa kalibracyjna absorbancja w funkcji %obj etanolu
|
Próbka |
T |
94,00 |
A |
0,02687 |
Etanol [%obj] |
5,4 |
Opracowanie:
Irena Štrumbelj Drusany, Alma Kapun Dolinar and Boštjan Ozimek, Biotehniški izobraževalni center Ljubljana
|