Zakaj je pomembno poznavanje zgradbe atomov?
V prejšnjem
poglavju si se naučil(a), da sestavljajo atome elementov v jedru protoni in
nevtroni, elektroni pa se nahajajo v elektronski ovojnici.
V tem poglavju pa
boste spoznali:
- kaj je vrstno
in masno število,
- kaj je izotop
določenega elementa,
- kaj je
radioaktivnost in kakšen je njen pomen za človeka,
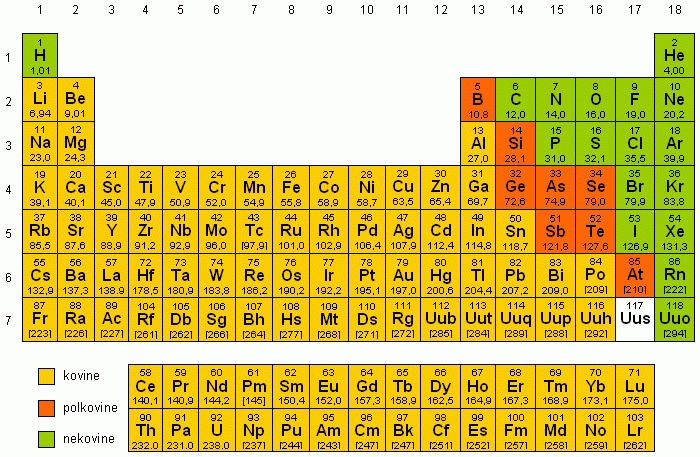
Za vsak atom določenega elementa je značilno točno določeno vrstno ali atomsko število. Vrstna števila elementov so običajno zapisana v periodnem sistemu elementov nad simbolom elementa. Vrstno število je število protonov (ali elektronov) v atomu in podaja tudi zaporedno mesto, kjer se v periodnem sistemu določen element nahaja.
Masnih števil običajno ni zapisanih v periodnem sistemu elementov. Masno število določa vsota vseh protonov in nevtronov v jedru atoma. Določen element ima lahko atome z različnim masnim številom. Pod simbolom elementov so zapisane relativne atomske mase, katerih pomen boste spoznali kasneje.
Periodni sistem elementov:
K imenom ali
simbolom elementov pripiši njihovo vrstno število.
Dušik ; Si ; kalij ; Br ; neon ; Sr ; magnezij
S pomočjo zapisa dopolni spodnje povedi. Pomoč: Zapis predstavlja sestavo jedra natrijevega atoma. Levo zgoraj je zapisano masno število, levo spodaj pa vrstno število.
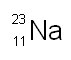
Natrijev atom ima
elektronov in
protonov. Navzven je atom natrija
, ker ima enako število
in elektronov. Vrstno
število natrija je
, masno število pa
. Natrijev atom ima
nevtronov v jedru. Število nevtronov izračunamo tako, da od
števila odštejemo
število.
Kateri pari simbolnih zapisov, označeni z X in Y predstavljajo izotope istega elementa?
V naravi se ne
nahaja enak delež vseh izotopov nekega elementa. Vodik se npr. lahko pojavi v
treh izotopih. Vodika (H), ki je brez nevtrona, je v naravi največ, okoli 99,98
%. Devterija (D) z enim nevtronom je v naravi manj kot 0,02 %. Najmanj je
tricija (T), ki se v naravi nahaja le v sledovih, ima pa dva nevrona v jedru.
Tricij ima masno
število
, devterij pa
. Vodik, tricij in
devterij imajo
število elektronov in protonov, in sicer
.
Jedrska sila, ki
delujejo med nevtroni in protoni v jedru je zelo močna. Odbojne sile med
pozitivno nabitimi protoni bi lahko brez vmes vrinjenih nevtronov povzročile,
da bi jedro razpadlo. Jedrska sila je tako močnejša od odbojnih sil in zato
drži jedro skupaj, da ne razpade zlahka. Jedra atomov so večinoma stabilna,
nekatera z velikim številom delcev v jedru (več kot 83 protonov), pa lahko tudi
spontano razpadejo. Taki elementi nimajo stabilnih izotopov. Jedro pa lahko
tudi razpade, če se vanj vrinejo dodatni nevtroni, zato atomi izotopov
elementov pogosto razpadejo. Jedro atomov lahko razpade na manjša jedra, ali pa
se zlijejo manjša jedra v večja. Pri tem nastanejo atomi drugih elementov. Ker
se je spremenilo jedro atoma, pravimo, da poteče jedrska reakcija. Jedrske
reakcije so lahko spontane ali pa umetno spodbujene. Spontane jedrske reakcije
potekajo, pri radioaktivnem razpadu elementov (razpad atoma urana na atom torij
in atom helij) ali pri zlivanju atomov, ki poteka v zvezdah (dva atoma vodika
se zlijeta v atom helija). Pri jedrskih reakcijah se sprosti veliko energije v
obliki radioaktivnega sevanja. Sevanje je lahko v obliki delcev (jedra atomov
helija ali elektroni) ali energije (gama žarki).

Eksplozija jedrske bombe nad Nagasakijem na Japonskem, kar je pomenilo kapitulacijo Japonske (vir: Wikipedia).
Radioaktivno
sevanje je zelo nevarno saj ima veliko energijo in prodre globoko v tkiva ter
poškoduje dedni material. Jedrsko orožje je zelo nevarno. Le enkrat je bilo
jedrsko orožje uporabljeno v vojne namene. Dve atomski bombi sta eksplodirali
nad Hirošimo in Nagasakijem na Japonskem leta 1945, kar je pomenilo zaključek
2. svetovne vojne. Pri dolgotrajni izpostavljenosti bolj nizkim dozam sevanja
lahko pride do nastanka različnih vrst raka ali poškodb nerojenega zarodka
ljudi in živali. Pri kratkotrajni izpostavljenosti velikim dozam sevanja pa
pride do opeklin kože in poškodb notranjih organov. Radioaktivno sevanje je
lahko smrtno nevarno. Radioaktivno sevanje pa se uporablja tudi v medicini za
rentgensko slikanje in različne preiskave (npr. preiskave delovanja žleze
ščitnice z radioaktivnim jodom) in geologiji in arheologiji, pri ugotavljanju
starosti kamnin ali predmetov (razpad atomov ogljika, glej animacijo).
Kateri element nastane pri radioaktivnem razpadu atomov ogljika z masnim številom 14?
|
Stabilen atom ogljika z masnim številom 14.
| |
|
Stabilen atom dušika z masnim številom 14.
| |
|
Stabilen atom ogljika z masnim številom 12.
| |
|
Nestabilen atom dušika z masnim številom 15
|
Elementi, kot so
vodik, dušik, kisik in elementi v 17. (VII.) skupini periodnega sistema, pogosto tvorijo dvoatomne
molekule, beli fosfor tvori štiriatomne, žveplo pa osematomne molekule.
Pravilno Nepravilno
Pravilno Nepravilno
Pravilno Nepravilno
Pravilno Nepravilno
Pravilno Nepravilno
