Lastnosti in funkcije beljakovin
Spoznali boste, zakaj so beljakovine oz. proteini izrednega pomena za življenje.
Spoznali boste eno od pomembnih lastnosti beljakovin – koagulacijo.
Podrobneje boste spoznali funkcije štirih skupin beljakovin: strukturne, transportne in obrambne beljakovine ter encime.
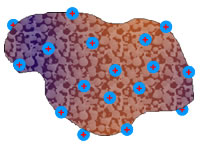
V vodi so nekatere beljakovine (predvsem nitaste) netopne in tvorijo gel. A tudi topne beljakovine (kroglaste beljakovine) se v vodi ne topijo tako kot kuhinjska sol ali sladkor. Za razliko od sladkorja, ki se v vodi razgradi na posamezne molekule, ali natrijevega klorida, ki se v vodi loči na posamezne ione, beljakovine vežejo na svojo površino ione z enakim nabojem. Ti ioni povzročijo, da se beljakovine med seboj odbijajo ali privlačijo – odvisno od naboja, ki je vezan na površini posamezne molekule beljakovine. Odboj oz. privlak med beljakovinami pa omogoča, da se beljakovine, kljub svoji velikosti, ne usedajo na dno. Vodotopne beljakovine tvorijo koloidno raztopino.

|
|
| Površina molekule beljakovine, na katero so vezani anioni. |
Površina molekule beljakovine, na katero so vezani kationi. |
Gel: heterogena zmes snovi, v katerem delci snovi niso prosto gibljivi in imajo zato precej stalno obliko.
Koloidna raztopina: heterogena zmes snovi, v katerih je ena snov fino razpršena v drugi snovi. Razpršeni delci so tako majhni, da jih s svetlobnim mikroskopom ne moremo videti, prav tako jih ne moremo ločiti iz zmesi s filtrirnim papirjem, saj jih ta ne zadrži.
Jajčni beljak pri segrevanju zakrkne.
|
Kakšno temperaturo bodo beljakovine zdržale, je odvisno od njihove zgradbe. Dovajanje energije pri segrevanju povzroči prekinitev vezi v beljakovinskih molekulah. Šibke vezi razpadejo že pri temperaturi okrog 50 °C, močnejše pa pri daljšem segrevanju nad 50 °C.
|
 |
Ko se beljakovina pri segrevanju spremeni, rečemo, da zakrkne (se sesiri, se skepi) ali koagulira. To je pojav, da se beljakovina izloči (obori) iz raztopine. Koagulacijo beljakovin lahko dosežemo tudi na druge načine, npr. s kislinami in bazami (ki nevtralizirajo naboj na površini beljakovin), s solmi težkih kovin, drugimi beljakovinami (npr. belajkovine v kačjem strupu, sirilo) in z vrsto organskih spojin (alkoholi, alkaloidi). Spremembo lastnosti beljakovin pri koagulacij imenujemo denaturiranje beljakovin.
Do denaturacije beljakovin lahko pride tudi pri mešanju beljakovin, npr. pri stepanju jajčnih beljakov:
Pomemben dejavnik za obstojnost beljakovin je oblika beljakovin: nitaste so odpornejše kot kroglaste beljakovine.
|
|
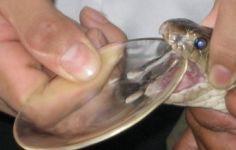
| Strupene kače so znane po izredno močnem strupu, ki ga vbrizgajo v plen, vendar so beljakovine v strupu tako občutljive, da postane strup neučinkovit že ob močnejšem stresanju raztopine. Vir slike: Barry Rogge (licenca: Priznanje avtorstva 2.0). |
Parklji, kopita, rogovi, nohti, kremplji, dlaka in perje so zgrajeni iz izredno odporne beljakovine keratin. Vir slike: Wikipedia. |
Kot veste iz svojih vsakdanjih izkušenj, spreminjanje beljakovin pod vplivom segrevanja ni vedno nezaželeno. Trdo surovo meso se zmehča, tekoč jajčni beljak postane trden, obenem pa s kuhanjem in pečenjem hrano steriliziramo, saj spremenimo beljakovine bakterij v hrani ter jih tako uničimo ali preprečimo njihovo razmnoževanje. V medicini s segretim električnim nožem povzročijo spremembe lastnosti beljakovin v žilah in s tem preprečijo krvavitve.
|
Koagulirane beljakovine ohranijo svoje lastnosti in obliko.
| |
|
Koagulacija je sprememba strukture beljakovin.
| |
|
Do koagulacije pride le pri močnem segrevanju beljakovin.
|
Sladkor.
| |
Natrijev hidroksid.
| |
Žveplova kislina.
| |
Natrijev klorid.
| |
Kobaltov sulfat.
| |
|
Ker pride do povečanega izločanja vode iz telesa, kar lahko povzroči dehidracijo.
| |
|
Ker se v krvi pojavijo mehurčki hlapnih snovi, kar vodi v moten pretok kisika do celic.
| |
|
Ker lahko pride pri tako visoki temperaturi do spremembe zgradbe beljakovin.
|
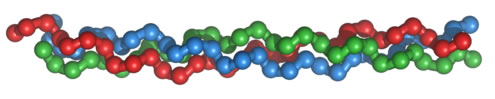
Model molekule kolagena. Molekula je sestavljena iz treh polipeptdinih vlaken. Vir: Wikipedia.
|
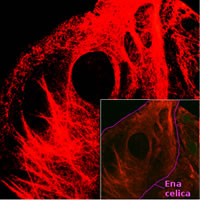
Keratin je eden izmed najtrši materialov, iz katerih so zgrajeni organizmi. Gradi nohte, kremplje, perje, kopita, parklje. Keratin vsebuje veliko žvepla in je odporen na encime, ki razgrajujejo beljakovine. Slika levo: mikroskopski posnetek nitastih struktur keratina v celici (rdeča barva). Vir: Wikipedia. |
|
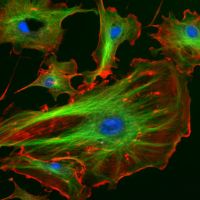
Nitaste in zelo odporne strukture lahko nastanejo tudi iz globularnih
beljakovin. Aktin in tubulin sta globularni vodotopni beljakovini,
vendar pri polimerizaciji tvorita dolge, toge nitaste strukture. |
|
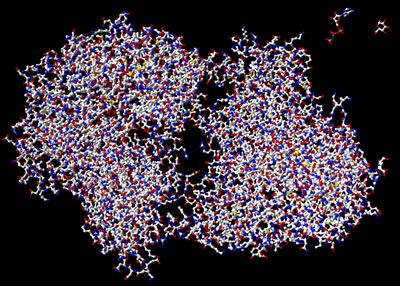
Slika desno: model človeškega hemoglobina. Modri in rdeči deli predstavljajo beljakovinski del hemoglobina. Zeleno obravani deli vsebujejo atome železa. Vir: Wikipedia. |

|
|
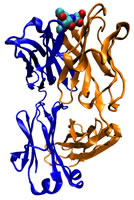
Za konec omenimo še obrambne beljakovine. Najznačilnejša so antitelesa iz skupine imunoproteinov. To so globularne beljakovine, s katerimi se organizem brani pred napadi bakterij in virusov. Antitelesa se vežejo na različne snovi, ki se nahajajo na površini bakterij in virusov (te snovi se imenujejo antigeni) ter preprečijo, da bi škodovali organizmu. Slika desno: Mišje antitelo proti koleri. Antitelo je predstavljeno z modrimi in rumenimi trakovi. Kalotni model predstavlja antigen. Vir: Wikipedia. |
|
Keratin:
Hemoglobin:
Kolagen:
Polimeriziran tubulin:
Imunuproteini:

Ime encima je sestavljeno iz imena substrata, na katerega encim deluje oz. reakcije, ki jo katalizira ter končnice -aza:
- laktaza - encim, ki razgrajuje laktozo.
- DNK polimeraza - encim, ki katalizira polimerizacijo vijačnice DNK.
V telesu potekajo skoraj vse reakcije pod vplivom encimov (doslej je poznanih okrog 4000 reakcij, ki jih katalizirajo encimi). Delovanje encimov je specifično; to pomeni, da vsak encim katalizira le nekaj reakcij ali le eno samo. Nazoren primer za specifično delovanje encimov je presnova škroba in celuloze v organizmih. Čeprav sta tako škrob in celuloza zgrajena iz tisočev molekul glukoze, so te med seboj povezane na drugačen način, zato se encim za razgradnjo celuloze razlikuje od encima za razgradnjo škroba. Encima za razgradnjo celuloze ljudje nimamo, zato ne moremo prebaviti celuloze.
Način delovanja encimov lahko pojasnimo z modelom imenovanim „rokavica – roka“. Po tem modelu so encimi sposobni, da se do določene mere prilagajajo različnim velikostim in oblikam molekul, podobno kot se rokavice prilagajajo različnim rokam, seveda do določene mere. En del molekule encima se lahko delno razteguje, zato se nanj vežejo različne molekule, med drugim tudi tiste, ki ovirajo delovanje encima.
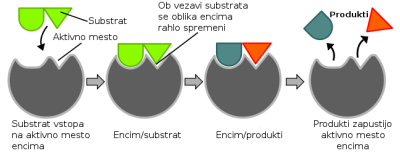
Encimi imajo precej zapleteno zgradbo. Skoraj vsi so globularne beljakovine. Nekateri encimi potrebujejo za delovanje še dodatne snovi – kofaktorje, ki so anorganske (npr. kovinski ion) ali organske snovi.
Kroglični model encima v primerjavi z modeloma molekul ATP in glukoze (zgoraj levo). Vir: Wikipedia.
|
Encimi so v organizmih zastopani v izredno majhnih količinah, vendar so te majhne količine dovolj za normalno delovanje organizmov, saj encim ostane po poteku reakcije nespremenjen in lahko takoj nato sproži drugo enako reakcijo. Encimi so izredno občutljivi, ker so zgrajeni iz globularnih molekul in ne trajajo večno. Encimi v telesu neprenehoma razpadajo, telo jih nadomešča tako, da izdela nove.
|
 |
 |
In kaj se zgodi, če se encimi uničijo ali izgubijo sposobnost kataliziranja reakcij, telo pa jih ne more nadomestiti? Živi organizmi so v celoti odvisni od delovanja encimov. Če karkoli ovira njihovo delovanje, to lahko pomeni smrt za organizem. Običajno mora biti uničenih veliko encimov v daljšem časovnem obdobju, da do tega sploh pride, vendar obstajajo tudi encimi, ki so za življenje organizma tako ključnega pomena, da že nekajminutno oviranje njihovega delovanja pomeni za organizem pogubo. In nekateri strupi že v zelo majhnih količinah (npr. vodikov cianid) povzročajo prav to. Encimi niso pomembni zgolj za delovanje organizmov. Pomembni so tudi v biotehnologiji. Že od antičnih časov jih človeštvo uporablja pri pridobivanju vina, piva in kruha (spomnite se na encime kvasovk) ter sira. Dandanes se poleg uporabe v živilski tehnologiji, uporabljajo še pri proizvodnji zdravil, energije, najdemo pa jih tudi v pralnih praških in zobnih pastah. |
|
Katalizator katalizira veliko različnih kemijskih reakcij.
| |
|
Katalizatorji zvišajo energijo, ki je potrebna, da se reakcija sproži.
| |
|
Katalizator je snov, ki omogoča, da reakcija hitreje in lažje steče, sam pa se pri reakciji ne porablja.
| |
|
Encimi so zelo obstojni, njihove količine v telesu so majhne.
|
A laktoza:
B amiloza (in amilopektin; oba sta sestavini škroba):
C polimerizacija DNK vijačnice: