Snovi so iz delcev
Na osnovi poskusov boste spoznali, da so snovi zgrajene iz nevidnih delcev. V tekočinah in plinih se delci stalno gibljejo. Za lažje razumevanje lahko delce snovi ponazorimo z modeli. Modele bomo uporabili za ponazoritev porazdelitev delcev v trdnih snoveh, tekočinah in plinih. To je tudi izhodišče za prikaz prehodov med agregatnimi stanji. Tako bomo lažje razumeli, da se pri tem snovi ne spremenijo, spremeni se le oblika v kateri so odvisno od temperature in tlaka. V isti snovi so enaki delci ne glede na agregatno stanje snovi.
Raztapljanje kalijevega manganata v vodi.
V valj nalijemo 250 mL vode, ki ji dodamo nekaj kristalčkov kalijevega manganata. Voda se pri stiku s kalijevim manganatom obarva vijolično, tako da lahko vidimo, kako kristalčki padajo proti dnu valja. Čez čas kristalčkov kalijevega manganata ne vidimo več, ker so se v vodi raztopili. Vsa tekočina v valju se je obarvala vijolično. Snovi so zgrajene iz delcev. V vodni raztopini so delci kalijevega manganata, ki jo obarvajo vijolično.
Če raztopino dobro pomešamo, je barva vse raztopine enaka. Delci kalijevega manganata so se v raztopini enakomerno porazdelili.
Razredčevanje vodne raztopine kalijevega manganata.
Raztopino kalijevega manganata razredčujemo z vodo. V epruveto nalijemo 1 mL raztopine kalijevega manganata in ji dodamo 9 mL vode. Iz dobljene raztopine vzamemo 1 mL in mu dodamo 9 mL vode. To ponavljamo dokler je dobljena raztopina še obarvana. Obarvanje je odvisno od števila delcev kalijevega manganata v raztopini.
|
Kondenzacija.
| |
|
Izhlapevanje.
| |
|
Koncentriranje.
| |
|
Razredčevanje.
|
Primerjamo raztopini kalijevega manganata z različno jakostjo obarvanja.
|
V obeh raztopinah je raztopljena enaka količina kalijevega manganata.
| |
|
Barva raztopine ni odvisna od količine vode v njej.
| |
|
V močno obarvani raztopini je raztopljenega več kalijevega manganata kot v šibko obarvani.
| |
|
V močno obarvani raztopini je manj delcev kalijevega manganata kot v šibko obarvani.
|
Brom je pri sobni temperaturi tekočina. Iz nje izhajajo rdečkasti hlapi broma, ki se širijo po prostorni posode. Prostornina valja ni enakomerno obarvana. Ob tekočem bromu je barva rdečkasta, nato pa je po valju navzgor vse svetlejša.
Čez čas se celotna prostornina obarva. Brom je sestavljen iz delcev, ki izhajajo iz tekočega broma in se gibljejo v prostornini valja.
|
Hlapi broma izhajajo iz tekočega broma.
| |
|
Iz obarvanja ne moremo sklepati na količino par broma v valju.
| |
|
V valju delci broma mirujejo.
| |
|
Hlapi broma niso obarvani.
|
Snovi so v vseh agregatnih stanjih sestavljene iz majhnih nevidnih delcev. Premer teh delcev merimo v nm (nano metri), kar pomeni 0,000000001 m in v pm (piko metrih), kar pomeni 0,000000000001 m. Za opazovanje teh delcev uporabljamo elektronski mikroskop in druge še bolj občutljive metode.
Za lažjo predstavo kako veliki so delci snovi, so podane merske enote.
| Oznaka | Pomen | Primer |
| kilo (k) |
103 1000 | 1 km = 103 m |
| deci (d) |
10-1 0,1 | 1 dm = 0,1 m |
| centi(c) | 10-2 0,01 | 1 cm = 0,01 m |
| mili (m) |
10-3 0,001 | 1 mm = 0,001 m |
| mikro (μ) | 10-6 0,000001 |
1 mikrometer 1 μm = 0,000001 m |
| nano (n) | 10-9 0,000000001 |
1 nanometer 1 nm = 0,000000001 m |
| piko (p) | 10-12 0,000000000001 |
1 pikometer 1 pm = 0,000000000001 |
Merska skala
| Makro skala |
Mikro skala |
Nano skala |
|||||||
| 1 m |
1 dm |
1 cm |
1 mm |
100 μm | 10 μm | 1 μm | 100 nm |
10 nm |
1 nm |
Glede na velikost razvrsti na mersko skalo:
velikost odraslega človeka uvrščamo na skalo,
velikost delcev v sladkorju uvrščamo na skalo,
velikost rastlinske celice uvrščamo na skalo,
velikost lista pisarniškega papirja uvrščamo na skalo,
velikost delcev v vodi uvrščamo na skalo.
Ista snov je odvisno od temperature in tlaka lahko trdna, tekoča ali plin. Rečemo, da je v trdnem, tekočem in plinastem agregatnem stanju. Delci snovi so v vseh treh agregatnih stanjih enaki, različna je le njihova razporeditev in njihova hitrost gibanja.
V trdnih snoveh se delci močno privlačijo in na mestih kjer so, lahko le nihajo sem ter tja. Trdne snovi imajo zato določeno obliko in določeno prostornino. V trdnih snoveh so delci najbolj urejeni v primerjavi z delci v tekočinah in plinih.
Nihanje delcev:
Pri segrevanju se delci v trdni snovi gibljejo vedno hitreje, med seboj se vse manj privlačijo in snov se začne taliti. Iz trdne snovi nastane tekočina.
Taljenje:
|
Težji delci se hitreje gibljejo od lažjih.
| |
|
Hitrost gibanja delcev ni odvisna od temperature.
| |
|
Pri isti temperaturi se lažji delci hitreje gibajo od težjih.
| |
|
Pri segrevanju snovi se delci v njej počasneje gibajo.
|
V tekočinah se delci manj privlačijo in se lahko bolj prosto gibljejo kot v trdnih snoveh. Njihovo gibanje je omejeno s prostornino tekočine. Tekočine nimajo oblike. To določa oblika posode v kateri so.
Gibanje delcev
Pri segrevanju tekočin izhajajo iz njih delci snovi. Iz tekočine nastane plin. V plinih se delci gibajo zelo hitro in so med seboj precej oddaljeni. Plin nima niti določene prostornine niti določene oblike.
Gibanje delcev
Kako imenujemo proces pri prehodu plina v tekočino?
Kako imenujemo proces pri prehodu trdne snovi v tekočino? .
|
V isti snovi so v različnih agregatnih stanjih različni delci.
| |
|
V trdnih snoveh se delci prosto gibljejo.
| |
|
Delci so med seboj v plinih bolj oddaljeni kot v tekočinah.
| |
|
Hitrost gibanja delcev iste snovi je v vseh agregatnih stanjih enaka.
|
Na sliki je voda v treh agregatnih stanjih. Dane so tudi porazdelitve delcev v ledu, tekoči vodi in vodni pari, ki so označene s številkami.
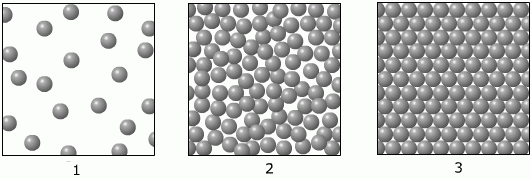
V ledu so porazdeljeni delci tako kot je prikazano na shemi . Porazdelitev delcev v tekoči vodi je enaka porazdelitvi delcev na shemi . V vodni pari so porazdeljeni delci tako kot je prikazano na shemi .
Podane so ponazoritve delcev v različnih agregatnih stanjih snovi. Ob posamezni porazdelitvi napiši številko agregatnega stanja, ki jo porazdelitev ponazarja.
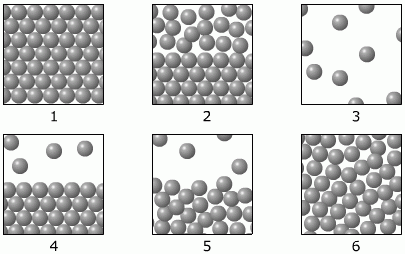
plin; tekočina; trdna snov; plin in tekočina; trdna snov in tekočina;
plin in trdna snov
Na sliki so podane porazdelitve delcev v agregatnih stanjih vode. Delci v ledu, tekoči vodi in vodnih hlapih se enaki, različna je le njihova porazdelitev. V tekoči vodi se delci počasneje gibljejo kot v vodnih hlapih. Delci v ledu ne mirujejo, temveč nihajo okrog dolečenih leg v strukturi.

Porazdelitev delcev na sliki ponazarja vode.

Porazdelitev delcev na sliki ponazarja ledu.