Standardna sprememba entalpije pri fizikalnih procesih
Med fizikalne procese spadajo npr. sprememba agregatnega stanja snovi, raztapljanje in razredčevanje. Tako kot kemijske reakcije so tudi fizikalni procesi povezani s spremembo energije v obliki toplote, ki jo imenujemo standardna sprememba entalpije; navedemo pa tudi, za kateri proces gre.
Sprememba agregatnega stanja snovi je enostavnejši fizikalni proces.
Standardna talilna entalpija vode 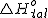 je npr. sprememba entalpije pri procesu
taljenja enega mola ledu pri 100 kPa in tališču vode, ki je 0 oC
oziroma 273,15 K. Proces je endotermen, ker je potrebno toploto dovajati.
Podobno velja za izparevanje.
je npr. sprememba entalpije pri procesu
taljenja enega mola ledu pri 100 kPa in tališču vode, ki je 0 oC
oziroma 273,15 K. Proces je endotermen, ker je potrebno toploto dovajati.
Podobno velja za izparevanje.
Oglejte si poskus in odgovorite na spodnja vprašanja.
Proces taljenja ledu
lahko opišemo z enačbo:
H2O(s) → H2O(l)
Za ta proces znaša
standardna talilna entalpija 6,01 kJ/mol pri 273,15 K.
Izberite pravilni odgovor.
|
Taljenje je eksotermen proces.
| |
|
Za stalitev dveh molov ledu je potrebno dovesti
12,02 kJ toplote.
| |
|
Pri taljenju masla v ponvi se energija sprošča.
| |
|
Za strditev ledu je potrebno energijo
dovesti.
|
Strjevanje je proces, kjer preide tekočina v trdno snov. Temu procesu rečemo v primeru vode tudi zmrzovanje. Proces poteka torej v nasprotni smeri, kot poteka taljenje - toplota se pri strjevanju sprošča.
Koliko toplote se sprosti pri strjevanju enega mola tekoče vode pri 0 oC?
|
3,05 kJ
| |
|
6,01 kJ
| |
|
9,06 kJ
| |
|
12,0 kJ
|
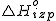 je sprememba
entalpije pri procesu izparevanja enega mola tekočine pri 100 kPa in temperaturi vrelišča tekočine.
je sprememba
entalpije pri procesu izparevanja enega mola tekočine pri 100 kPa in temperaturi vrelišča tekočine.
Proces izparevanja
npr. vode lahko opišemo z enačbo:
H2O(l) → H2O(g)
Za ta proces znaša standardna izparilna entalpija 40,6 kJ/mol pri 100 oC. Katera trditev je pravilna?

Gejzir. Vir: Wikipedia.
|
Izparevanje je eksotermen proces.
| |
|
Za izparevanje dveh molov
tekoče vode je potrebno dovesti 60 kJ toplote.
| |
|
Pri izparevanju etanola
se energija sprošča.
| |
|
Za izparevanje enega mola vode je potrebno dovesti
40,6 kJ energije v obliki toplote.
|
Kondenzacija imenujemo proces, pri katerem preide snov iz plinastega agregatnega stanja v tekoče agregatno stanje. Ta proces je obraten procesu izparevanja. Pri kondenzaciji se toplota sprošča.
Koliko toplote se sprosti pri kondenzaciji enega mola metanola pri 100 kPa in 337,2 K?
|
70,6 kJ
| |
|
106 kJ | |
|
35,3 kJ
| |
|
17,6 kJ
|
